华大在线讯(通讯员 朱潇潇)近日,我校化学学院孙耀教授课题组和犹他大学Stang教授课题组合作在病原菌的精准诊治方面取得了重要进展,相关研究成果发表在国际权威综合类化学期刊《德国应用化学》(Angewandte Chemie International Edition, 2021,doi.org/10.1002/anie.202110048)上,华中师范大学一年级博士生徐玉玲为论文的第一作者,孙耀教授为最后通讯作者。
抗菌药物滥用导致了细菌耐药已经对全球公共卫生安全构成了重大威胁。设计可快速标记、精准示踪病原菌感染的荧光探针,是减少抗生素滥用和实现病原菌精准诊治的前提。现有的有机小分子荧光探针在示踪过程中往往存在自身聚集导致荧光淬灭的现象,因而极大的干扰了荧光成像检测的精准度。孙耀课题组另辟蹊径从分子调控入手,设计柱芳烃修饰的超分子大环Pt作为主体分子(1),以荧光小分子作为客体分子(2),通过其主客体相互作用构筑了新型超分子荧光探针1⊃2(图1)。
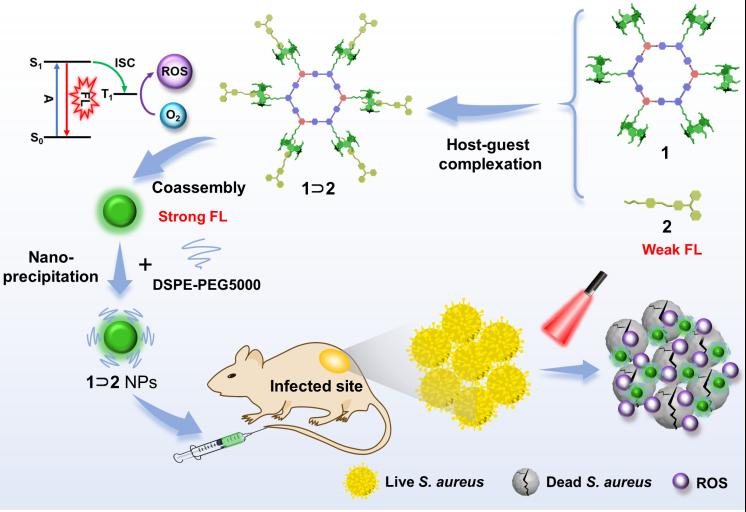
通过主体大环的刚性及主客体作用“双管齐下”的策略,一方面最大程度限制了荧光小分子2化学键的转动和振动及减少非辐射跃迁;另一方面降低了荧光分子间的堆积作用及避免了荧光的淬灭效应,从而显著提升了超分子荧光探针1⊃2的荧光和光动力性能(图1)。体外光物理性能表征结果显示超分子荧光探针1⊃2的荧光强度和单线态氧量子产率相对于荧光小分子2分别提升了85倍及40%,且其性能远优于市面上商品化的小分子光敏剂二氢卟吩Ce6。随后的理论计算也进一步的证实了“双管齐下”的策略可以显著降低其HOMO-LUMO轨道及激发单重态(S1)-激发三重态(T1)之间的能级差。
基于上述性能优势,超分子荧光探针1⊃2能够在体外快速、精准标记病原菌,原位引发光动力抗菌,在低剂量下能够选择性杀死金黄色葡萄球菌,而对正常哺乳细胞呈现低毒性。随后,该探针在活体上快速“点亮”病原菌感染区域,通过荧光成像引导光动力原位杀灭病原菌且对感染的伤口进行高效的修复。这项工作为今后发展生物医学应用的超分子荧光试剂提供了新的设计思路。
(审读人:王海)