华大在线讯(通讯员 朱潇潇)近日,化学学院吴安心教授课题组与广东医科大学郑恺鹭博士协作,成功在I2-DMSO组合试剂介导下实现了一例三组分的新型串级环化反应,高效构建具有季碳中心的吡咯[2,1-a]异喹啉衍生物。该工作以“I2-DMSO Mediated Multicomponent [3+2] Annulation Reaction: An Approach to Pyrrolo[2,1-a]isoquinoline Derivatives with a Quaternary Center”为题发表在Organic Letters(DOI: 10.1021/acs.orglett.2c03651)上。论文第一作者为我校化学学院2019级博士研究生庄诗怡,通讯作者为吴安心教授与广东医科大学郑恺鹭博士。
吡咯并异喹啉骨架作为一种重要的有机杂环结构,广泛存在于许多天然产物、生物碱和生物活性分子之中。研究表明,许多吡咯并[2,1-a]异喹啉衍生物在体外表现出良好细胞毒性和抗肿瘤活性。由于其广泛的生物活性,此类化合物的合成也引起了化学家极大的研究兴趣(图 1)。
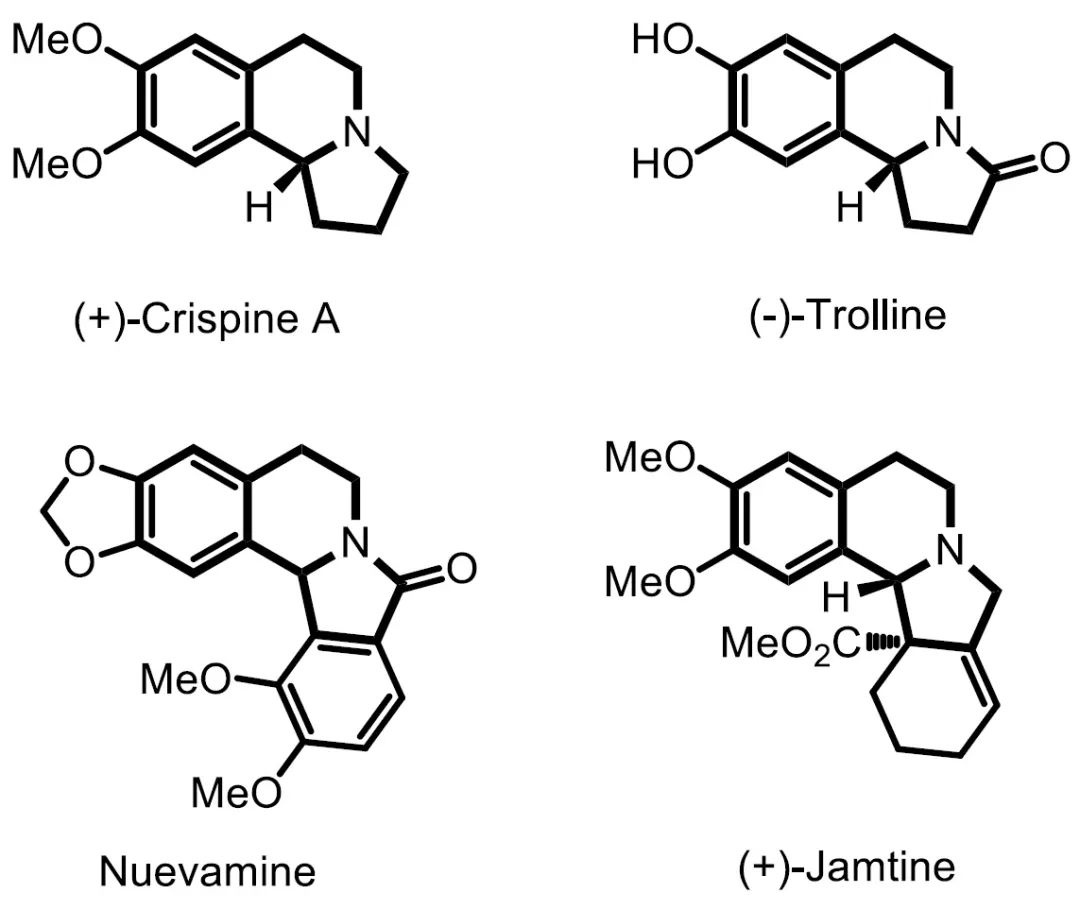
图1. 具有生物活性的吡咯并[2,1-a]异喹啉衍生物
(图片来源:Organic Letters)
近年来,C−C键的断裂在有机合成中得到了广泛的关注,因为其能够使得原有的结构发生重建与重组形成新的骨架单元。然而由于C−C键具有非极性、相对惰性、热力学和动力学稳定性的特点,C−C键的断裂面临着巨大的挑战。通过释放小环的环张力可以为C−C键的断裂提供额外的驱动力,从而使其C−C键断裂能够在温和的条件下发生。
环丙烯酮作为一类已知的符合Hückel芳香性的最小单环化合物,在配体、生物合成中间体和聚合物交联剂等领域表现出广泛的应用性。由于环丙烯酮具有两亲性,在有机合成中可将其作为2C/3C合成子,发生[2+n]/[3+n]环化反应,构建多样化的杂环化合物。其中,在金属或有机催化条件下,通过环丙烯酮的C−C键断裂将其作为3C合成子参与[3+2]环加成反应得到了快速的发展。例如,2019年李兴伟教授团队报道了一例镍催化下环丙烯酮与α,β-不饱和酮/亚胺的[3+2]环化反应,合成具有高度对映选择性的γ-烯基丁烯内酯和内酰胺衍生物(图2a)。此外,Patureau教授课题组于2022年发展了一例三苯基膦催化下环丙烯酮与苯并噁唑的去芳构化[3+2]环加成反应(图2b)。发展更加温和的催化方法将进一步丰富环丙烯酮C−C键活化的应用范围,并提高其实用性和可持续性。基于此,作者在I2-DMSO介导的条件下成功实现了环丙烯酮C−C键断裂与开环并将其作为三元合成子参与[3+2]环化过程,于一锅之中构建带有季碳中心的吡咯并[2,1-a]异喹啉衍生物。该反应成功实现了1,2,3,4-四氢异喹啉的N−H/α-C(sp3)−H的三官能团化,并于一锅之中构建两个C−C键和一个C−N键(图2c)。
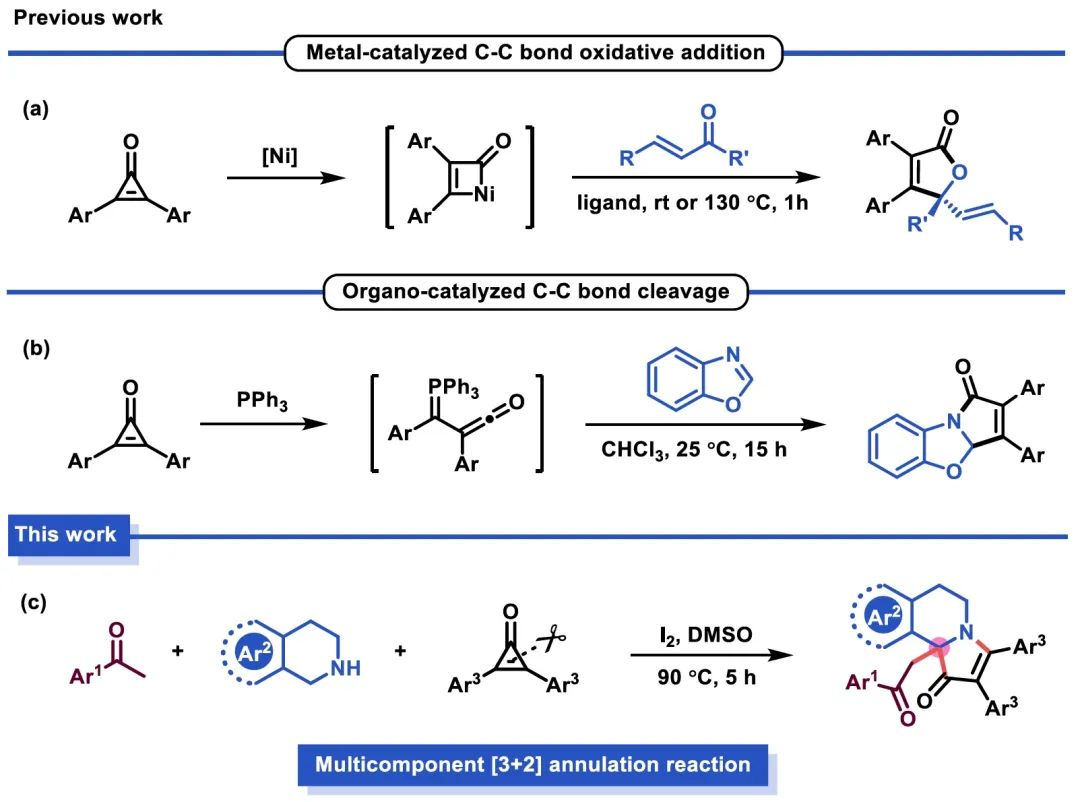
图2.环丙烯酮参与的[3+2]环化反应
(图片来源:Organic Letters)
为了优化反应收率,作者以苯乙酮、四氢异喹啉和二苯基环丙烯酮作为模型底物对反应条件进行了筛选,发现在添加1.2当量碘的情况下于90 ℃的DMSO中反应5小时,能够以71%的收率得到目标产物。
在确立了最优的反应条件后,作者对反应的底物兼容性进行了考察。首先,对于给电子基取代的苯乙酮(Me, Et, OMe, OEt, 3,4-OCH2O, SMe),能够以57%–69%的收率得到目标化合物(4a–4m)。当选用吸电子基团取代的苯乙酮(CO2Me, CN, NO2)作为反应底物时,并不会对反应收率造成明显影响(4n–4q)。卤素取代的苯乙酮能良好地兼容于该反应(4r–4x),将芳基乙酮的苯环替换为其他杂环或大位阻芳环时,反应也能够顺利进行(4y–4ae)。
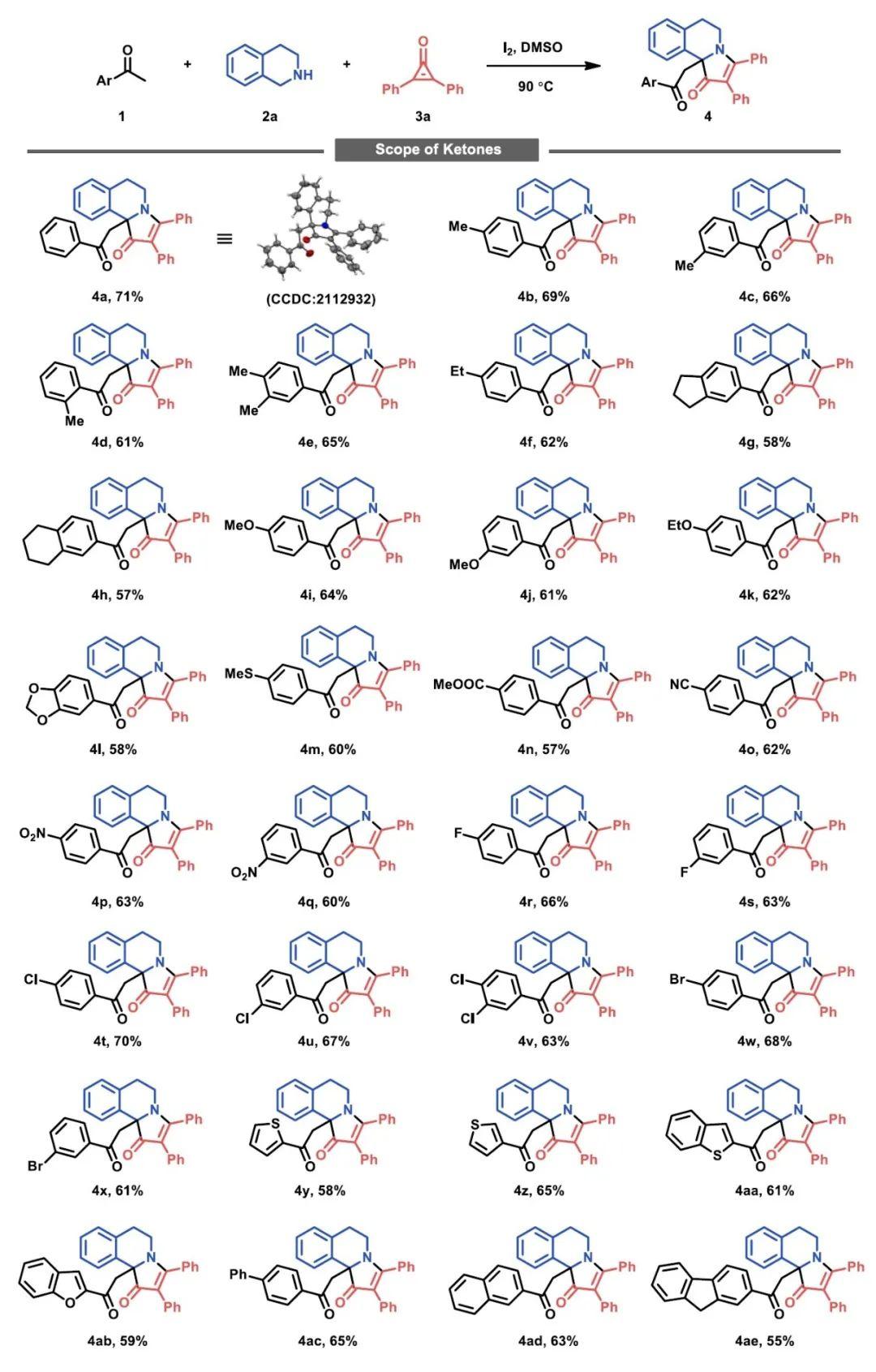
图4. 四氢异喹啉与环丙烯酮的底物普适性考察
(图片来源:Organic Letters)
为了探究该反应可能的反应机理,作者进行了一系列的控制实验研究。在I2-DMSO介导的条件下,苯乙酮(1a)能够以定量的收率转化为芳基酮醛(1ab)及其对应的水合物(1ac)(图5a)。在标准条件下,α-碘苯乙酮(1aa)能够与四氢异喹啉(2a)、二苯基环丙烯酮(3a)反应,表明1aa可能是该反应的中间体(图5b)。然而,芳基酮醛(1ab)并不能参与这种转化(图5 c)。将2a单独置于标准条件下反应时,能够通过GC-MS检测到3,4-二氢异喹啉(5)的存在(图5d),且当选用3,4-二氢异喹啉(5)取代四氢异喹啉(2a)参与反应时,能够以75%的收率得到目标化合物4a(图5e)。以上结果表明3,4-二氢异喹啉(5)可能是反应中间体。氩气气体保护实验表明空气中的氧气可能不参与四氢异喹啉(2a)的氧化步骤(图5f)。最后,在不添加碘的情况下,化合物6能够与1aa和3a反应,进一步验证了1aa和亚胺离子6可能是反应中间体(图5g)。

图5. 机理探究实验
(图片来源:Organic Letters)
基于上述的控制实验和相关的文献报道,作者提出了可能的反应机理(图6)。首先,四氢异喹啉(2a)发生碘代过程得到中间体A,随后消去一分子HI生成亚胺中间体5。与此同时,苯乙酮(1a)经碘代生成α-碘代苯乙酮(1aa),再与亚胺中间体5反应生成亚胺离子中间体6。中间体6随后失去一个质子和一个碘负离子,得到甲亚胺叶立德中间体B并发生互变异构生成中间体C。中间体C进攻另一分子的α-碘代苯乙酮(1aa)得到中间体D。中间体D再次发生互变异构生成中间体E,并在碘负离子的作用下脱去一分子α-碘代苯乙酮,得到中间体F。中间体F亲核进攻二苯基环丙烯酮(3a)生成中间体G,最后再经历分子内环化反应生成目标化合物4a。
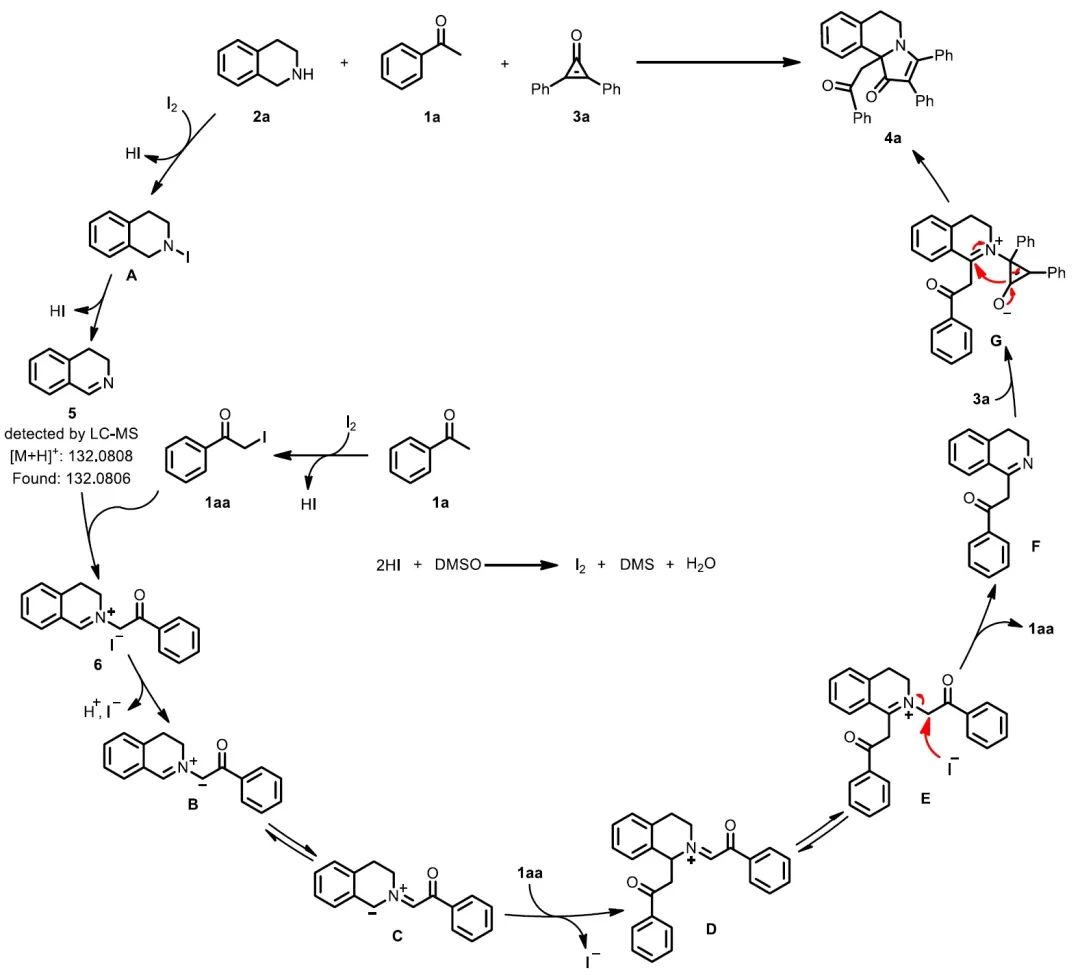
图6. 可能的反应机理
(图片来源:Organic Letters)
综上所述,作者以芳基乙酮、四氢异喹啉以及环丙烯酮为起始反应原料,在I2-DMSO组合试剂介导下实现了带有季碳中心的吡咯并[2,1-a]异喹啉骨架的高效构建。值得注意的是,该反应涉及一个C−C键的断裂和多个新化学键的构建,成功地实现了四氢异喹啉N−H/α-C(sp3)−H的三官能团化。在这一反应中,环丙烯酮能够在温和条件下发生C−C键断裂并开环,不仅开发了其全新的反应模式,还进一步丰富了其作为3C合成子的应用场景。
该项研究工作得到了国家自然科学基金、广东省基础与应用基础研究基金省市联合基金、广东省医学科研基金、广东医科大学博士科研基金的大力支持。
(审读人:王海)